Acquisto
Acquista l’apparecchiatura di convalida di Ellab ed esegui autonomamente studi di convalida, in qualsiasi momento e luogo.
Rentals
Noleggia l’apparecchiatura di Ellab e prova i prodotti prima di concludere l’acquisto.
Servizio in loco
Usufruisci di servizi di qualifica e convalida in loco. Disponiamo di ingegneri di convalida formati ed estremamente competenti.
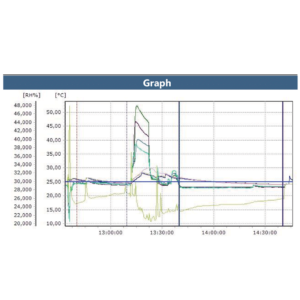
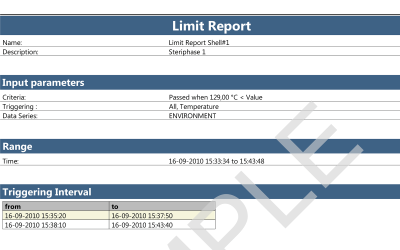
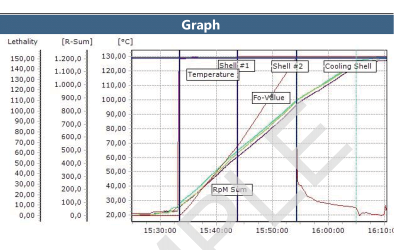
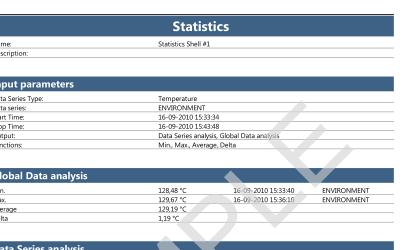
Report del software ValSuite®
Camera di stabilità