Equipment kaufen
Führen Sie Ihre Messaufgaben flexibel mit einem eigenen Validierungssystem durch – jederzeit und egal wo.
Equipment mieten
Mieten Sie Ellab-Messequipment und überzeugen Sie sich von zahlreichen Features, die Ihre Arbeit erleichtern.
On-Site Service & Consulting
Gerne unterstützen wir Sie vor Ort bei der Qualifizierung Ihrer Anlagen und der Prozessvalidierung sowie -optimierung.
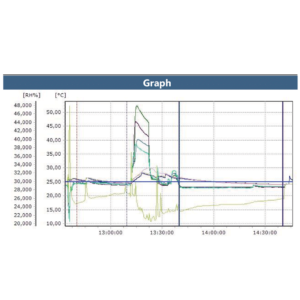
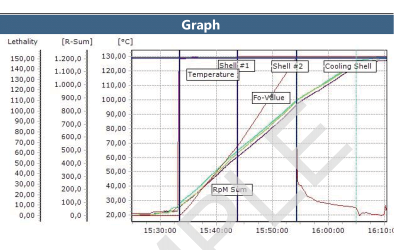
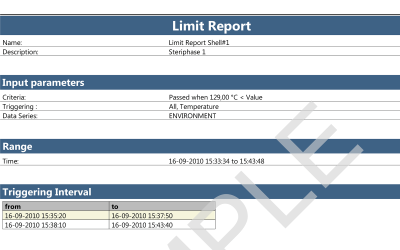
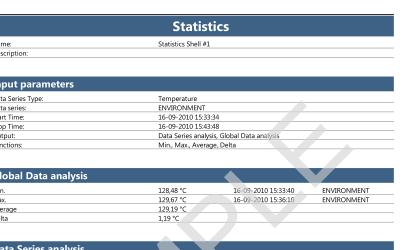
ValSuite® Software Reports
Stabilitätskammer