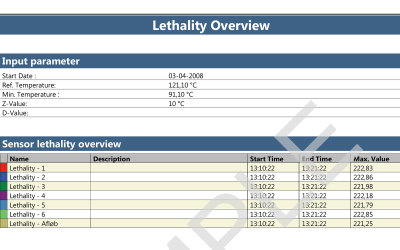
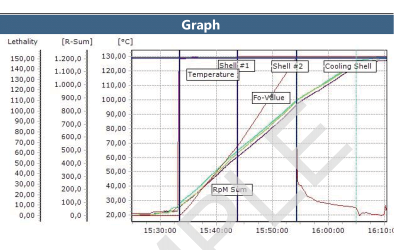
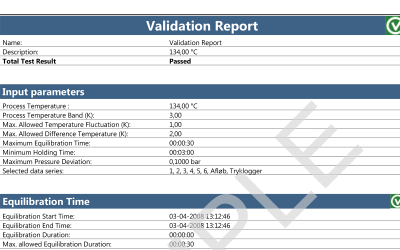
Sowohl kabellose Datenlogger als auch Thermoelementsysteme sind eine geeignete Wahl, wenn es um Qualifizierung und/oder Validierung von Dampfsterilisation und Autoklaven geht.
Kabellose Logger sind aufgrund des RTD-Sensordesigns sehr genau und stabil, was sie zur idealen Option für die Qualifizierung des Autoklaven und die Validierung des Dampfsterilisationsprozesses macht.
Ein kabelgebundenes Thermoelementsystem kann ebenfalls verwendet werden und ist anfangs möglicherweise die wirtschaftlichere Option, erfordert jedoch letztendlich mehr Ressourcen für den Betrieb – was zu Herausforderungen führt, die durch die Verwendung eines kabellosen Systems vermieden werden könnten. Dies ist darauf zurückzuführen, dass kabellose Datenlogger im Vergleich viel einfacher einzurichten und zu steuern sind.
Bei Verwendung eines kabelgebundenen Thermoelementsystems zur Autoklavenvalidierung besteht die zusätzliche Herausforderung darin, die Druck- und Vakuumintegrität aufrechtzuerhalten. Dafür kann ein Feed-Through verwendet werden. Das Feed-Through-System von Ellab wurde ausgiebig getestet, um minimale Leckage und optimale Qualifizierungseffizienz zu gewährleisten.